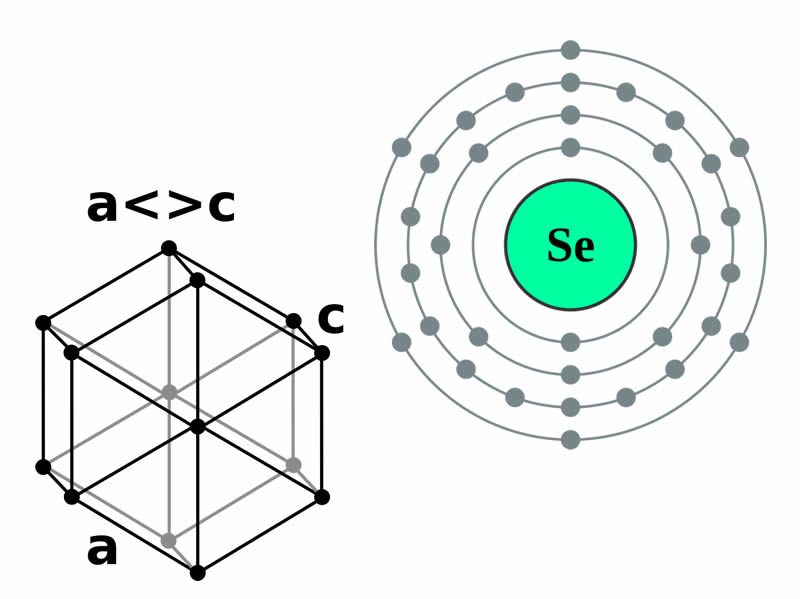
El selenio se puede preparar con una estructura amorfa o cristalina. El selenio cristalino es profundamente rojo; el selenio es hexagonal cristalino, la variedad más estable, es un gris metálico. El selenio elemental es relativamente no tóxico y se considera un elemento esencial para la vida. Sin embargo, el seleniuro de hidrógeno (H2Se) y otros compuestos del selenio son extremadamente tóxicos, y se asemejan al arsénico en sus reacciones fisiológicas. El seleniuro de del hidrógeno en una concentración de 1.5 PPM es intolerable para los seres vivos. Los suelos que contienen cantidades altas pueden producir efectos serios sobre la alimentación de animales y de las plantas.
Datos esenciales:
|
|
Descripción:
- Estado estándar: sólido en 298 grados kelvin
- Color: lustre gris, metálico
- Clasificación: No-metálico
- Disponibilidad:
[whitespace]
El selenio se puede preparar con una estructura amorfa o cristalina. El selenio cristalino es profundamente rojo; el selenio es hexagonal cristalino, la variedad más estable, es un gris metálico. El selenio elemental es relativamente no tóxico y se considera un elemento esencial para la vida. Sin embargo, el seleniuro de hidrógeno (H2Se) y otros compuestos del selenio son extremadamente tóxicos, y se asemejan al arsénico en sus reacciones fisiológicas. El seleniuro de del hidrógeno en una concentración de 1.5 PPM es intolerable para los seres vivos. Los suelos que contienen cantidades altas pueden producir efectos serios sobre la alimentación de animales y de las plantas.
[header_title title=”Aislamiento” header_size=”h4″]
No es generalmente necesario obtener el selenio en el laboratorio pues está comercialmente disponible. En la mayoría de los casos, el selenio se lo obtiene como subproducto de la refinación de cobre. También se acumula en los residuos de la fabricación del ácido sulfúrico. La extracción es compleja, puesto que el método empleado dependerá de que compuestos o elementos estén presentes. El primer paso implica generalmente una oxidación en la presencia del carbonato de sodio.
Cu2SE + Na2Co3 + 2O2 → 2CuO + Na2SeO3 + Co2
El Na 2SeO3 de la selenita se acidifica con el ácido sulfúrico. Cualquier precipitante de los teluros deja el ácido seleniuro, H2SeO3, en la solución. El selenio es liberado del ácido seleniuro por TAN2
H2SeO3 + 2SO2 + H2O → SE + 2H2TAN4
El selenio (Gr. Selen, moon) fue descubierto por Jöns Jacob Berzelius en 1817. Él divulgó que el telurio estaba presente en el ácido sulfúrico de una fábrica sueca, pero en el año siguiente descubrió que la impureza no era telurio sino otro elemento muy relacionado y lo identificó posteriormente como selenio.
[header_title title=”Formas químicas:” header_size=”h4″]
|
FLUORUROS |
CLORUROS |
BROMUROS |
OXIDOS |
SULFUROS |
|
SeF2 |
SeCl2 |
SeBr |
SeO2 |
Se4S4 |
|
FSeSeF |
Se2Cl2 |
SeBr2 |
SeO3 |
Se2S6 |
|
SeSeF2 |
[SeCl4]4 |
Se2Br2 |
||
|
SeF4 |
[SeBr4]4 |
NITRUROS |
||
|
SeF6 |
Se4N4 |
[header_title title=”Usos comunes” header_size=”h4″]
El selenio tiene una acción Fotovoltaica, donde la luz se convierte directamente en electricidad, y la acción fotoconductora, donde la resistencia eléctrica disminuye con la iluminación creciente. Estas características hacen el selenio útil en la producción de fotocélulas, cintas fotográficas y fotocopiadoras, así como las células solares.
El selenio puede también convertir la electricidad de corriente alterna a corriente continua y se utiliza extensivamente en reguladores de voltaje, es un tipo semiconductor y es útil en electrónica.
[header_title title=”El selenio como elemento esencial para la vida” header_size=”h4″]
El selenio es esencial para los seres vivos, especialmente para los mamíferos, plantas, pero solamente en cantidades pequeñas. El selenio sirve principalmente para estimular el metabolismo.
El metabolismo para muchos organismos, incluyendo a los peces, la materia y la energía son suministradas por sustancias orgánicas como carbohidratos, proteínas, grasas, que sufren algunas transformaciones para ayudar a los organismos a cumplir sus funciones vitales. A estas transformaciones se les denomina como metabolismo por lo tanto, metabolismo se podría definir como el conjunto de cambio de sustancias y transformaciones de energía que tiene lugar en los seres vivos.
El selenio es un micronutriente para todas las formas de vida conocidas que se encuentra en el pan, los cereales, el pescado, las carnes y los huevos. Es antioxidante, ayuda a neutralizar los radicales libres, induce la apoptosis (muerte celular programada ), estimula el sistema inmunológico e interviene en el funcionamiento de las glándulas. Está presente en el aminoácido selenocisteina.
El término antioxidante significa que impide la oxidación perjudicial de otras sustancias químicas, ocasionada en las reacciones metabólicas o producidas por los factores exógenos como las radiaciones ionizantes.
Un radical libre es una molécula (orgánica o inorgánica), en general extremadamente inestable y, por tanto, con gran poder reactivo. Se pueden formar en la atmósfera por radiación, y también se forman en los organismos vivos (incluido el cuerpo del pez) por el contacto con el oxígeno y actúan alterando a las membranas celulares y atacando el material genético de las células, como el ADN.
Las investigaciones realizadas han mostrado la existencia de una correlación entre el selenio y la Vitamina E.
[header_title title=”Vitamina E” header_size=”h4″]
Llamada también tocoferol, esta vitamina liposoluble esencial para el organismo de los seres vivos es también un antioxidante que ayuda a proteger los ácidos grasos. Así cuida al organismo de la formación de moléculas tóxicas resultantes del metabolismo normal como de las ingresadas por vías respiratorias o bucales. Evita la destrucción anormal de glóbulos rojos, evita trastornos oculares, anemias y ataques cardíacos. La absorción depende de la capacidad para digerir y absorber los lípidos.
Tanto la bilis como las enzimas pancreáticas son esenciales para su absorción. Se deposita lentamente en el hígado, músculo y principalmente en el tejido adiposo.
[header_title title=”Resumen de Funciones del selenio:” header_size=”h4″]
- Potente antioxidante: previene y retrasa el envejecimiento, previene la oxidación de las grasas que forman estructuras nerviosas o la membrana celular de todas las células
- Unido a la vitamina E se potencian
- Mejora la elasticidad de los tejidos y los protege
- Gran amigo del corazón: proporciona oxígeno a las células cardiacas, se puede usar en cualquier problema cardiovascular
- Ayuda a la reproducción.
- Favorece la fertilidad en ambos sexos unido a la vitamina E
- Mejora el crecimiento de los organismos juveniles
- Potencia y estimula el sistema inmunológico creando anticuerpos
- Favorece el buen funcionamiento del hígado y lo protege de su degeneración grasa
- Mejora el estado de la piel y mucosas: intestinal, respiratoria
- Ayuda en el ejercicio y la función muscular
- Mejora el estado del cristalino y de la retina del ojoFavorece la eliminación de urea y ácido úrico
El selenio, la vitamina E y la vitamina C. en forma conjunta y coordinada detienen la toxicidad de los radicales libres. Cada antioxidante posee una afinidad hacia un determinado RL o hacia varios.
La vitamina E, el betacaroteno y el licopeno actúan en el medio liposoluble de la célula y su absorción y transporte se hallan muy vinculados con el de los lípidos. La vitamina E es considerada el más importante protector de las moléculas lipídicas.
Vitamina C: neutraliza el oxígeno singlete, captura radicales hidroxilos, captura anión hiperóxidos y regenera la forma oxidada de vitamina E.
Glutatión peroxidasa: esta enzima intracelular contiene Selenio, remueve los radicales peróxidos. Es detoxificante.
Vitamina E: neutraliza el oxígeno singlete, captura radicales libres hidroxilos, neutraliza peróxidos y captura anión superóxido.
Betacaroteno: neutraliza el oxígeno singlete.
Es necesaria la incorporación al organismo de ciertos oligoelementos como el cobre, hierro, cinc, selenio y manganeso, pues forman parte del núcleo activo de las enzimas antioxidantes. Los llamados oligoelementos enzimáticos catalizan o aceleran reacciones químicas que utilizan sustratos que a su vez reaccionan con los radicales libres. Selenio: otro mineral antioxidante importante para la acción de la enzima glutation peroxidasa y de la vitamina E. También se ha sugerido que el selenio participa en la biosintesis de ubiquinona (coenzima Q, involucrada en el transporte electrónico intracelular) e influencia la absorción y retención de la vitamina E.
[header_title title=”Fuentes dietéticas y absorción” header_size=”h4″]
Fuentes dietéticas ricas en selenio incluyen solubles deshidratados de pescado, harina de pescado (5-2 mg/kg Se); levadura seca de cerveza, harina de gluten de maíz, levadura seca de tórula, harina de nabo, harina de semilla de algodón (2-1 mg/kg Se); y granos secos de destilería, salvado de trigo, trigo medianero, harina de lino, harina de pluma hidrolizada, harina de productos secundarios de aves, harina de carne y de alfalfa (1-0.5 mg/kg Se). El selenio es absorbido del tracto gastrointestinal y del agua del medio circundante tanto por peces como crustáceos.
|
Especie/elemento |
Requerimiento dietético (%) |
Referencia |
| SELENIO | ||
| Trucha arco-iris (S. gairdneri) | 0.07–0.38 mg/kg | Hilton, Hodson & Slinger (1980) |
| Bagre de canal (I. punctatus) | 1–5 mg/kg 1 | Gatlin & Wilson (1984) |
[header_title title=”Fuentes literarias” header_size=”h4″]
- J.E. Huheey, E.A. Keiter, y R.L. Keiter en química inorgánica: Principios de la estructura y de la reactividad, 4ta edición, HarperCollins, Nueva York, los E.E.U.U., 1993.
- N.N. Bosque verde y A. Earnshaw en la química de los elementos, 2da edición, Butterworth, Reino Unido, 1997.
- F.A. Algodón, G. Wilkinson, C.A. Murillo, y M. Bochmann, en química inorgánica avanzada, Juan Wiley y Sons, 1999.
- D.R. Lide, (ed.) en el manual de Chemical Rubber Company de la química y de la física, prensa del CRC, Boca Raton, la Florida, los E.E.U.U., 77.a edición, 1996.
- R.T. Sanderson in Chemical Periodicity, Reinhold, New York, USA, 1960.
- N.N. Greenwood and A. Earnshaw in Chemistry of the Elements, 2nd edition, Butterworth, UK, 1997.
- F.A. Cotton, G. Wilkinson, C.A. Murillo, and M. Bochmann, in Advanced Inorganic Chemistry, John Wiley & Sons, 1999.
- A.F. Trotman-Dickenson, (ed.) in Comprehensive Inorganic Chemistry, Pergamon, Oxford, UK, 1973.
- R.W.G. Wyckoff, in Crystal Structures, volume 1, Interscience, John Wiley & Sons, 1963.
- A.R.West in Basic solid state chemistry Chemistry, John Wiley & Sons, 1999.
- A.F. Wells in Structural inorganic chemistry, 4th edition, Oxford, UK, 1975.
- J.D.H. Donnay, (ed.) in Crystal data determinative tables, ACA monograph number 5, American Crystallographic Association, USA, 1963.
- D.R. Lide, (ed.) in Chemical Rubber Company handbook of chemistry and physics, CRC Press, Boca Raton, Florida, USA, 77th edition, 1996.
- J.W. Mellor in A comprehensive treatise on inorganic and theoretical chemistry, volumes 1-16, Longmans, London, UK, 1922-1937.
- J.E. Macintyre (ed.) in Dictionary of inorganic compounds, volumes 1-3, Chapman & Hall, London, UK, 1992.
- García JC, García B, Morin MA, Céspedes EM, Clapes S, Etienne O. Radicales libres: impacto médico. BEB (México) 1993;13(3):75-83.
- Halliwell B, Gutterioge JMC. Free radical in biology and medicine. Oxford: Clarendon, 1989;1:142.
- Freeman BA, Crapo JD. Free radicals and tissue injury. Lab Invest 1982;47:412-5.
- Basaga HS. Biochemical aspects of free radicals. Biochem Cell Biol 1989;68:989-98.
- Reilly PM, Bulkley GB. Tissue injury by free radicals and other toxic oxygen meyabolites. Br J Surg 1990;77:1324-5.
- Witztum JI. Role of oxidised low density lipoprotein i atherogenesis. Br Heart J 1993;69:12-8.
- Turrens J. Fuentes intracelulares de especies oxidantes en condiciones normales y patológicas. Antioxidante y Calidad de Vida 1994;1:16-9.
- Market M, Andrew PC, Babiar BM. Measurement of superoxide production by human neutrophils. Methods Enzimol 1984;105:358-65.
- Gerschman R. Oxigen poisoning and X-Irradiation. A mechanism in common. Science 1954;119:623-6.
- Oteiza PA. Modificación activa de las proteínas. Antioxidante y Calidad de Vida 1995;2:12-20.
- Tzu Chen Yen, Kwam Liang King, Hish Chen Lee. Age dependent increase of mitochondrial DNA deletions together with lipid peroxide and superoxide dismutase in human liver mitocondria. Free Radic Biol Med 1994;16:207-14.
- Sohal RS, Sohal BH, Orr WC. Mitochondrial superoxide and hydrogen peroxide generation, protein oxidative damag, and longevity in different species of flies. Free Radic Biol Med 1995;19:499-504.
- Orr WC, Sohal RJ. Extension of life-span by overexpression of superoxide dismutase and catalase in drosophila melanogester. Science 1994;263:1128-30.
- Tosaki A, Droy-Lefaix MI, Pali L, Das DK. Effects of SOD, catalase and a novel antiarrhythmic drug; EGB 761 on reperfusion induced arrythmias in isolated rat hearts. Free Radic Biol Med 1993;14:361-70.
- Left JA, Parson PE, Day CE. Increased serum catalase activity in septic patients with the adult respiratory distress syndrome. Am Rev Respir Dis 1992;146:985-9.
- Kawada T, Kambara K, Arakawa M. Pretreatment with catalase of dimethyl sulfoxide protects alloxan-induced acute lung edema in dog. J Appl Physiol 1992;73:1326-33.
- Zini A, De Lamirande E, Gagnon C. Reactive oxygen species in semen of infertile patients: levels of superoxi dismutase and catalase like activitier in seminal plasma and spermatozoa. Int J Androl 1993;16:183-8.
- Stepanik TM, Ewing DD. Isolation of glutathione peroxidase, catalase and superoxide dismutase of human erytrocites. J Biochers Biophys Meyh 1993;20:157-69.
- Salonen JJ. Risk of cancer in relation to serum concentrations of selenium and Vit. A and E. Matched case control analysis of prospectivedata. Br Med J 1985;290:417-20.
- Black G. Fruit vegetables and cancer prevention: a review of epidemiological evidence. Nutr Cancer 1992;18:1-29.
- Burr ML. Antioxidants and cancer. J Human Nutr Dietetics 1994;7:409-16.
- Esterbawer H, Gebicki J, Puhl H, Jurgens G. The role of lipid peroxidation and antioxidants in oxidative modification of LDL. Free Radial Biol Med 1992;13:341-90.
- Packer L. Vitamin E is nature´s master antioxidant. Sci Am Sci Med 1994;1:54-63.
- Kushi LH, Folsom AR, Prineas RJ, Mink PJ, Wu Y, Bostick R. Dietary antioxidant vitamins and death from coronary heart disease in postmenopausal women. N Engl J Med 1996;334;1156-62.
- Hodis HN, Mack WJ, Labreel C, Hemphill L, Sevanian A, Johnson R, et al. Serial coronary angiographic evidence that antioxidant vitamin intake reduces progression of coronary artery atherosclerosis. JAMA 1995;273:1849-54.
- Stephens NG, Parsons A, Schofield PM, Kelly F, Cheesman K, Mitchisnon MJ, et al. Randomised controlled trial of Vit. E in patients with coronary disease: Cambridge Heart Antioxidant Study (CHAOS). Lancet 1996;347:781-6.
- The Alpha -Tocopherol Beta Carotene Cancer Prevention Study Group. N Engl J Med 1994;330:1029-35.
- Omen GS, Goodman GE, Thornquist MD. Effects of combination of beta carotene and Vit. A on lung cancer and cardiovascular disease. N Engl J Med 1996;334:1150-5.
- Hennekens CH, Buring JE, Manson JE, Stampfer M, Rosner B, Coor NR. Lack of effect of Long-term suplementation with beta carotane on the incidence of malignant neoplasms and cardiovascular disease. N Engl J Med 1996;334:1145-9.
- Nelson RL. Pretary iron and colorectal cancer risk. Free Radic Biol Med 1993;41:677-82.
- Packer L. Vit. E is nature´s maste antioxidant. Sci Am Sci Med 1994;1:54-63. Seddon JM, Ajani VA, Sperduto RD. Dietary carotenoids, Vit. A, C, and E and advance age-related macular degeneration. JAMA 1994;272:1413-20.
- Aejmelaus RT, Holm P, Kauskinen U, et al. Age related changes in the peroxyl radical scavenging capacity of human plasma. Free Rad Biol Med 1997;23:69-75.
- Wei YH, Kad SH, Lee HC. Simultaneous increase of mitochondrial DNA deletion and lipid peroxidation in human aging. Ann NY Acad Sci 1996;786:23-34.
- Luscesoli F, Fraga CG. Evaluación del estrés oxidativo. Antioxidante y calidad de vida 1995;1:8-13.
- Motchnik PA, Frei B, Ames BN. Measurement of antioxidants in human blood plasma. Int Methods Entymol 1994;234:269-79.
Páginas Web:
http://www.crss.water.ca.gov/docs/SeFactsp.pdf.
http://www.fao.org/docrep/field/003/ab492s/AB492S04.htm

