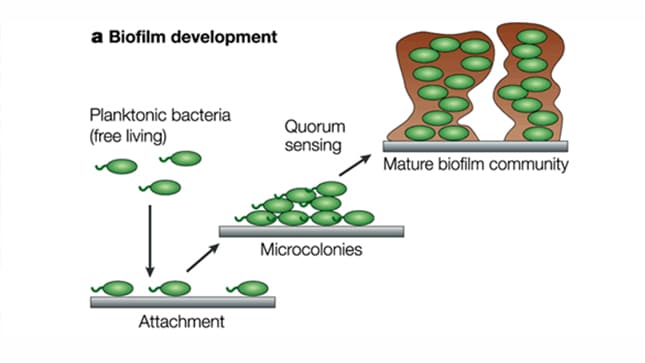
Resulta “normal” observar en el microscopio las bacterias libres (o planctónicas) moverse sobre una superficie, o en una muestra de agua, o en algún otro fluido; sin embargo, no siempre éste es su único estado natural, sino que se agrupan y se encierran dentro de biofilms (biopelículas) o matrices tridimensionales complejas, formadas por exo-polisacáridos. Los biofilms (también llamados glicocálix) pueden adherirse a una superficie inerte o viva (1). La comunicación de las bacterias planctónicas (o quorum sensing QS) está ligado a la formación de los biofilms. Las agrupaciones o colonias de bacterias que vemos en un plato de agar no es un amontonamiento al azar, sino que son estructuras de polímeros químicos extracelulares (mezcla de ADN, proteínas y polisacáridos) que forman el biofilm. Fig. 1. Las biopelículas presentan canales que permiten el flujo de agua, nutrientes y oxígeno.

Fig. 1. A través del QS las bacterias comparten información sobre la densidad celular y ajustar la expresión genética como consecuencia. [Ilustración tomada de internet.]
Las bacterias libres primero invaden los órganos del camarón, como la mucosa digestiva o los tejidos hepatopancreaticos y finalmente lo colonizan, formando biofilms. Las biopelículas resisten la acción de los antibióticos al no poder difundirse bien dentro de la matriz (2). Las infecciones causadas por bacterias que se encierran en biopelículas normalmente no consiguen ser completamente eliminadas, se vuelven recurrentes y pueden ser de 100 a 1.000 veces más resistentes a los antibióticos, que si esas mismas bacterias estuvieran libres en fluidos.
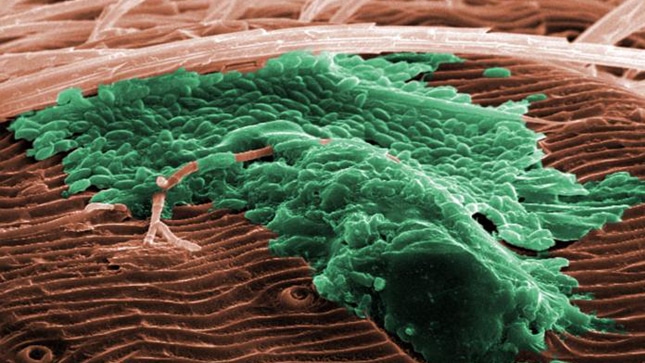
Fig. 2. Bacterias Gram-positiva y Gram-negativa usan diferentes tipos de sistemas QS. (Foto: Janice Haney Carr / CDC / Leah Lowrey, Michael Smith). Biofilm (en verde) sobre una superficie. Copyright © 1996-2017 Amazings® / NCYT® (Noticiasdelaciencia.com / Amazings.com). Lunes, 18 septiembre 2017.
Se considera que bajo condiciones ambientales adecuadas, todas las bacterias son capaces de formar biofilms, que les permiten superar la acción de fagocitos, sobrevivir a condiciones ambientales adversas y les ayudan a resistir los antibióticos, siendo los mecanismos responsables de esta resistencia:
- La barrera contra la penetración de los antibióticos.
- El crecimiento ralentizado de las bacterias dentro de la biopelícula por baja de nutrientes.
- La presencia de un ambiente que antagoniza con la acción antibiótica.
- La activación de respuestas de estrés, que provocan cambios en la fisiología de la bacteria y la aparición de un fenotipo específico del biofilm, que activamente combate los efectos negativos de los antibióticos (Mah y O’Toole, 2001).
Se debe tener en cuenta que los antibióticos utilizados rutinariamente han sido seleccionados por su efecto frente a bacterias libres y no a bacterias dentro de biopelículas; así mismo, los antibiogramas están diseñados para medir el efecto del antimicrobiano en bacterias crecidas de forma libre, y los resultados obtenidos pueden no ser extrapolables a esa misma bacteria cuando está creciendo en el interior de un biofilm (3).
Poco a poco se está suspendiendo el uso de antibióticos en la actividad acuicola y los núcleos orgánicos se presentan como una opción de antimicrobianos, para controlar bacterias patógenas que atacan al camarón en Ecuador. Surgen interrogantes:
¿Qué y cuál es la concentracion de ácidos orgánicos y aceites esenciales efectiva, para evitar eficientemente la formación de los biofilms y anular la acción patógena de las bacterias?.
¿Sera posible que una misma combinación de ácidos orgánicos y aceites esenciales sea suficiente para prevenir esas patologías?.
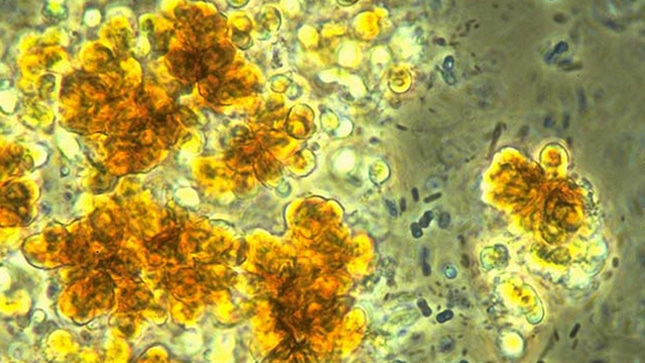
Fig. 3 Los biofilms aseguran la permanencia de las bacterias en el huésped, se adhieren y se resisten el desprendimiento.
https://wakeup-world.com/2013/03/10/infections-and-biofilms-what-are-they-and-what-lurks-in-them/
Consultas:
1. Scanning Electron Microscopy (SEM) and Environmental SEM: Suitable Tools for Study of Adhesion Stage and Biofilm Formation. Chapter 35. Book edited by Viacheslav Kazmiruk, ISBN 978-953-51-0092-8, Published: March 9, 2012 under CC BY 3.0 license. © The Author(s).
2. https://lacienciaysusdemonios.com/2010/06/13/imagenes-de-la-ciencia-y-la-naturaleza-biopeliculas-bacterianas/
3. Biofilms bacterianos. Íñigo Lasa Uzcudun. Instituto de Agrobiotecnología y Recursos Naturales y Departamento de Producción Agraria. Universidad Pública de Navarra. E-mail: ilasa@unavarra.es

